| Medusmaize, tik tiešām! |
[Apr. 29th, 2015|12:45 am] |
Sākās ta diena, kā diena - atradās kārtējais murgojums par sārmaino organismu. Iekš Tvnet jaunās sadaļas "Egoiste" (sadaļas saturs kopumā tāds pats, kā sadaļai "Sievietēm", tikai ar pamatīgu tendenci uz stulbumu). Par šo tēmu esmu izteicies iepriekš, un man jau sāk mazliet tā kā apnikt komentēt, bet tomēr atradu arī ko jaunu un negaidītu, par ko klusēt nu vienkārši nevaru.
Stāv tur rakstīts, ka "Hroniskas paskābināšanās ietekmē taukskābju negatīvie lādiņi mainās uz pozitīviem, tādēļ tās pielīp pie artēriju sieniņām, palielinot diabēta un sirds slimību risku". Tik konkrētiem ķīmiskiem terminiem, melns uz balta - bet tā kā ne visi ir labi pazīstami ar organisko skābju ķīmiju, atļaušos ilustrēt to, par ko tad šeit ir runa:
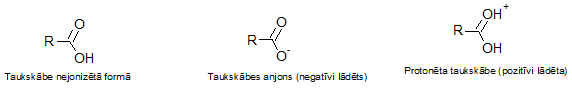
Taukskābju gadījumā burtiņa R vietā ir visai gara ogļūdeņražu aste, vienai taukskābei no otras šie fragmenti atšķiras ar, pirmkārt, garumu (t.i., to, cik oglekļa atomu ir saistījušies ķēdē), un otrkārt, ar to, kādas saites šos oglekļa atomus savā starpā savieno - ja visas ir vienkāršās saites, tad attiecīgo taukskābi pieskaita pie piesātinātajām, ja starp tām ir arī kāda dubultsaite vai vairākas, tad tā ir kāda no nepiesātinātajām taukskābēm. Tas gan ir mazsvarīgi konkrētajā gadījumā, jo visas lādiņu maiņas taukskābēm norisinās tieši attēlā redzamajā daļā - to sauc par karboksilgrupu.
Pa kreisi attēlota nejonizēta taukskābe - tā parasti pieraksta taukskābju (un arī citu karbonskābju) formulu. Tiesa, šādā formā taukskābes varētu būt nepolārā vidē - un ūdens vide (kāda ir mūsu organismā, piemēram), ir polāra. Tur skābes jonizējas. Un skābes tādēļ ir skābes, ka tās visai viegli atbrīvo pozitīvi lādētu ūdeņraža jonu (karbonskābju gadījumā - to, kurš ietilpst OH fragmentā), un atlikušais skābes fragments kļūst par negatīvi lādētu jonu (anjonu). Izņēmums varētu būt ļoti skāba vide - tajā jau ir tik liela pozitīvo ūdeņraža jonu koncentrācija, ka karbonskābe savējo atdot nespēj (vismaz formāli - reāli jau atdod gan, taču tikpat atri dabū citu vietā) Anjons attēlots turpat līdzās, un ir ļoti bieži sastopams fragments skābju šķīdumos ūdens vidē, pateicoties tam, ka atbrīvotais ūdeņraža jons spēj atgriezeniski saistīties ar ūdeni, turklāt skābes anjons gana viegli saistās arī ar citiem pozitīviem joniem (dažādu metālu katjoniem, piemēram). Un taisnības labad jāteic, ka brīvā formā taukskābes organismā nemaz tik bieži nav atrodamas (tās tur tiek transportētas saistītā formā kā triglicerīdi, un tiek atbrīvotas tikai noteiktos gadījumos, teiksim, lai izdabūtu cauri šūnu membrānām), taču jebkurā gadījumā, to anjons nav nekas eksotisks.
Nu, un var jau skābes arī iegūt pozitīvu lādiņu. Lai tas notiktu, karbonskābei ne vien jāsaglabā savs ūdeņraža atoms, bet papildus tam jāpiesaista viens "svešs" pozitīvs ūdeņraža jons. Struktūru uzzīmējis arī esmu, lai ilustrētu situāciju. Tā uzreiz no galvas nezināju, kādos apstākļos tad var veidoties šāds jons - protonēta karbonskābe ir visai reti sastopams zvērs. Droši tikai zināju, ka videi jābūt stipri skābai. Par laimi, eksistē skābju stipruma tabulas, un labākajās no tām var atrast arī to, cik tieši skābai. Te tiek lietots tāds lielums, kā pKa. Pārāk neiedziļināšos, teikšu tik, ka tas atbilst tādam pH (ekstrapolējot uz ūdens vidi), kurā attiecīgā skābe būtu par 50% disociējusi. Vai arī tā - jebkurš pH, kas mazāks par kādas skābes pKa vērtību, ir skābāks par to, un tāds, kas lielāks, attiecīgi, ir bāziskāks. Protonētās karbonskābes atrodas tuvu tabulas augšgalam, turpat, kur sālsskābe. To pKa ir ap -7. Tas nozīmē, ka tā ir apmēram 10^7 reizes stiprāka skābe, nekā ūdens vidē vispār varētu eksistēt - tā momentā protonētu ūdeni. Bet ja jums asinsvados sāktu plūst tīra sērskābe, tad jā, mierīgi. Tad visām jūsu taukskābēm būtu pozitīvs lādiņš. Tiesa, pie artēriju sieniņām tās diez vai pieliptu, jo nebūtu vairs tādu sieniņu - sērskābe tomēr nav nekāds joks, tā ir ļoti stipra neorganiska skābe. Ņemot vērā, ka līdz tādam asins skābumam cilvēkam aizdzīvoties nebūs iespējams, par pozitīvajām taukskābēm es atļaušos neuztraukties.
Ā, un beidzot atradu skaidrojumu tai citrona padarīšanai, vismaz pH diētas "speciālistu" izpratnē:
"Piemēram, lai gan citronu sula ir skāba, tā ķermeņa vidi padara sārmaināku, jo vielmaiņas procesā pārveidojas par bāzisku «citrātu»."
Un ja nu jums nav pa rokai citrona, nekrītiet izmisumā - droši pogājiet vaļā auto akumulatoru un tesiet tik iekšā. Bez bailēm, organismā sērskābe pārveidojas par bāzisku sulfātu. No lietām, kas vēl organismā tad pārveidojas, būtu minams rīkles dobums un barības vads, iesākumam. Bet nu, apgalvojums paliek ķīmiski korekts - sērskābe tik tiešām izveidos anjonu, kuru sauc par sulfātu (tāpat, kā citronskābes anjonu sauc par citrātu, bez pēdiņām). Un attiecīgais anjons pats par sevi pēc definīcijas ir bāziskāks par tam atbilstošo skābi, gan sērskābes, gan citronskābes gadījumā. Tas gan nemaina faktu, ka pirms kļūšanas par atbilstošo anjonu tā tomēr bija skābe, un lai kļūtu par anjonu, atdeva videi pozitīvi lādētu ūdeņraža atomu. Atšķirība starp abām šīm skābēm ir tā, ka sērskābe ir ļoti stipra skābe (atminamies, tās pKa = -9), un tādēļ spējīga savu ūdeņraža atomu momentā atdot da jebkam, kas par to ir jūtami bāziskāks (t.i., kā pKa ir lielāks par -9, kas organismā ir gluži vienkārši jebkas). Citronskābe ir švaka skābe, un organisma videi ūdeņraža atomu atdos nepilnīgi (proti, no visām citronskābes molekulām tikai kāda daļa, turlāt saglabāsies kaut kāds līdzsvars starp jonizēto un nejonizēto formu), rezultātā viegli pazeminot vides pH (ja tas jau tā nebūs aplam zems), atšķirībā no sērskābes, kas brutāli noprotonēs vienalga ko, un pat vārdu nepaprasīs, ne arī piedāvās kafiju iedzert... Tas gan faktu, ka abas ir skābes, nemaina, un no tā izriet, ka tās vides skābumu palielina, nevis samazina. Etiķskābe, piemēram, ir nedaudz švakāka skābe par citronskābi, un tā vides skābumu palielinās mazāk. Tālāk vielmaiņas procesā gan ar etiķskābes anjonu, gan citronskābes anjonu notiek šādas tādas pārmaiņas, taču neviena no tām, cik zinu, vidi bāzisku nepadara (ja kļūdos, lūgšu kādu zinošāku palabot - neizejot no bioloģijas rāmjiem ezotērikas virzienā, protams). Sērskābes anjonu gan pārāk interesanti piedzīvojumi negaida, bet nu, tas jau tā.
( Bet tas vēl nav viss, vēl tak medusmaize! ) |
|
|